이상기체 상태방정식 vs 보일-샤를 혼합방정식: 선택 기준
이상기체 상태방정식과 보일-샤를의 혼합 방정식을 선택할 때는 문제에서 제공되는 변수들을 고려해야 하며, 각 방정식이 다루는 범위와 가정에 따라 식을 선택하는 것이 좋습니다. 결과적으로는 비슷한 결과를 얻을 수 있지만, 상황에 따라 각 방정식이 좀 더 직관적이거나 계산에 편리할 수 있습니다.
1. 이상기체 상태방정식 (Ideal Gas Law)
이상기체 상태방정식은 다음과 같습니다:
![]()
여기서:
- P: 압력 (Pa 또는 atm)
- V: 부피 (m³)
- n: 몰 수 (mol)
- R: 기체 상수 (8.314 J/mol·K 또는 0.0821 L·atm/mol·K)
- T: 절대온도 (K)
사용할 때:
- 기체의 몰 수(n) 또는 기체 상수(R)를 포함하는 계산이 필요할 때.
- 기체가 이상기체로 가정되고, 온도, 압력, 부피 간의 관계를 계산할 때.
- 모든 변수(온도, 압력, 부피)가 주어졌거나 구해야 할 때.
2. 보일-샤를의 혼합 방정식 (Combined Gas Law)
보일-샤를의 혼합 방정식은 다음과 같습니다:
![]()
여기서:
- P1, P2: 초기 및 최종 압력
- V1, V2: 초기 및 최종 부피
- T1, T2: 초기 및 최종 온도 (절대온도 K)
사용할 때:
- 몰 수(n)나 기체 상수(R)가 문제에서 중요하지 않을 때.
- 기체가 변화하는 상태에서 압력, 부피, 온도 간의 관계를 계산할 때.
- 압력이 일정하거나, 온도나 부피의 변화를 다룰 때.
- 문제에서 온도, 부피, 압력의 초기 및 최종 값만 주어진 경우.
3. 어떤 변수를 고려해야 할까?
a) 몰 수(n)가 중요한가?
몰 수가 문제의 중요한 변수일 때, 이상기체 상태방정식을 사용하는 것이 더 적합합니다.
- 예를 들어, 일정한 몰 수의 기체에서 온도나 압력의 변화가 주어졌을 때, 이상기체 방정식은 직관적입니다.
b) 기체 상수(R)를 사용하는가?
기체 상수 ![]() 를 사용해야 한다면, 이상기체 상태방정식이 필수적입니다.
를 사용해야 한다면, 이상기체 상태방정식이 필수적입니다.
- 예를 들어, 기체가 특정 온도에서 주어진 몰 수일 때 부피나 압력을 계산하는 문제에서는 이 방정식이 필요합니다.
c) 변화하는 두 상태 간의 관계가 중요한가?
두 상태 간의 압력, 부피, 온도의 변화를 다루고, 몰 수나 기체 상수가 중요하지 않다면, 보일-샤를의 혼합 방정식을 사용하면 더 간단합니다.
- 예를 들어, 기체의 상태가 변할 때, 초기에 주어진 상태와 변형 후의 상태를 다루는 문제에서는 보일-샤를의 혼합 방정식이 적합합니다.
d) 온도 변화가 큰가?
온도의 변화가 크고, 압력이나 부피와의 관계를 다룰 때는 이상기체 상태방정식이나 보일-샤를 혼합 방정식 모두 사용할 수 있습니다. 그러나 상태 변화를 설명할 때는 혼합 방정식이 더 직관적일 수 있습니다.
4. 결과적으로 두 식은 동일한가?
결과적으로, 이상기체 상태방정식과 보일-샤를의 혼합 방정식은 같은 물리 법칙에서 유도된 식이므로, 특정 상황에서는 동일한 결과를 줍니다. 그러나 각 방정식은 다루는 변수와 상황이 다를 수 있습니다. 따라서 문제의 조건에 맞는 방정식을 선택하는 것이 중요합니다.
- 이상기체 상태방정식은 모든 변수를 다 다룰 수 있으며, 기체 상수
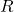 와 몰 수
와 몰 수 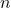 을 포함한 일반적인 계산에 적합합니다.
을 포함한 일반적인 계산에 적합합니다. - 보일-샤를의 혼합 방정식은 상태가 변하는 상황에서 더 간단하게 적용할 수 있으며, 압력, 부피, 온도 간의 변화를 직관적으로 계산할 수 있습니다.
따라서 주어진 문제에서 몰 수나 기체 상수가 중요한지 여부, 그리고 압력, 부피, 온도 간의 변화를 다루는 방식에 따라 방정식을 선택하는 것이 좋습니다.

